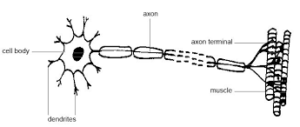
L’unité motrice
Elle est composée d’un motoneurone et des fibres musculaires qu’il innerve.
Le corps cellulaire des neurones moteurs
est situé dans la corne antérieure de la moelle. Les dendrites sont activés par les fibres du tractus pyramidal.
Les axones sont couverts d’une gaine de myéline, resserrée au niveau des noeuds de Ranvier (comme un chapelet de saucisses).
Chaque axone présente une ramification à son extrémité et un renflement terminal au contact de chaque fibre musculaire, formant la plaque motrice.
Normalement, les ramifications terminales ont des longueurs homogènes. A l’arrivée de l’influx nerveux, les signaux produits par l’activation des unités motrices sont à peu près synchrones et produisent un potentiel mono, di ou triphasique.
En pathologie, il peut y avoir une recolonisation d’unités motrices distantes : cela produit des potentiels polyphasiques de durée prolongée.
L’influx nerveux
Vidéo du Pr Ben Brahim Mohammed
Faculté de médecine et pharmacie, Fès (origine Youtube)
Le potentiel de repos
Entre l’intérieur et l’extérieur de la fibre nerveuse, il existe deux gradients, chimique et électrique.
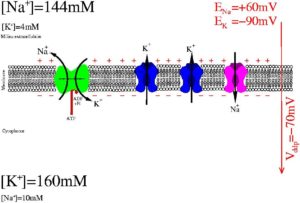 Le gradient chimique :
Le gradient chimique :
- Concentration supérieure de sodium Na + en extracellulaire,
- Concentration supérieure de potassium K+ en intracellulaire
Le gradient électrique :
- Au repos, membrane est peu perméable au Na+
- Elle pompe 3 Na+ vers l’extérieur contre 2 K+ vers l’intérieur.
- Ce pompage asymétrique fait gagner une charge + à l’extérieur
- K+ suit le gradient chimique : sort de la cellule. Le Na+ est bloqué à l’extérieur.
- L’intérieur de la membrane devient négatif, ce qui limite la diffusion de K+ à l’extérieur
Il en résulte un potentiel de repos : positif à l’extérieur, négatif à l’intérieur. Cette différence de potentiel est entretenu par les pompes à sodium et à potassium qui consomment de l’ATP comme source d’énergie.
A l’écran, ceci se traduit par une ligne de base stable.
Le potentiel d’action
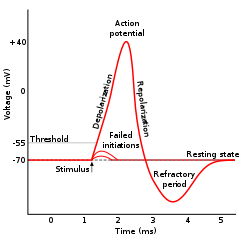 Le potentiel d’action est déclenché par une stimulation électrique qui doit dépasser un certain seuil. Au-dessous de ce seuil d’activation, les phénomènes électriques sont avortés et l’influx électrique ne se propage pas.
Le potentiel d’action est déclenché par une stimulation électrique qui doit dépasser un certain seuil. Au-dessous de ce seuil d’activation, les phénomènes électriques sont avortés et l’influx électrique ne se propage pas.
Au-dessus du seuil d’excitation, il se produit une cascade de phénomènes électrochimiques :
- Ouverture des canaux à Na+ qui laissent entrer le sodium dans la cellule, d’où une dépolarisation soudaine ; le potentiel d’action.
- Ouverture des canaux à K+ qui fait retomber la différence de potentiel et provoque une période réfractaire absolue durant laquelle on ne peut pas provoquer un deuxième potentiel d’action.
- Hyperpolarisation tardive due au pompage de Na+/K+ et période réfractaire relative.
Le potentiel d’action ne peut se maintenir sur place, mais excite l’axone de proche en proche : c’est l’onde de dépolarisation. La vitesse de propagation augmente avec le calibre des fibres. Les grosses fibres sont les plus rapides.
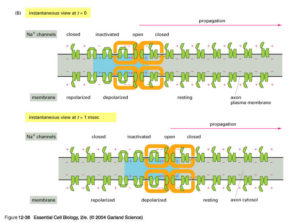 La conduction saltatoire
La conduction saltatoire
La gaine de myéline isole les axones, sauf au niveau des nœuds de Ranvier où des différences de potentiels peuvent s’établir. L’onde de dépolarisation ne va plus se propager de manière continue le long de l’axone, mais directement d’un nœud à l’autre, ce qui est beaucoup plus rapide : c’est la conduction saltatoire.
La conduction saltatoire est absente ou altérée :
- dans les fibres C qui véhiculent la douleur. Ce sont des petites fibres amyéliniques. Cela explique le retard de la sensation douloureuse, lors d’une piqûre ou d’une brûlure, par exemple.
- les neuropathies démyélinisantes, souvent par des phénomènes auto-immuns affectant la myéline.
- les syndromes canalaires et les ischémies transitoires. A noter que les fibres myélinisées sont moins résistantes que les fibres C
- la régénération après lésion axonale : la gaine de myéline est de qualité moindre et la conduction ralentie.
La jonction neuromusculaire
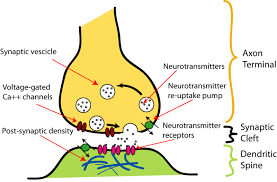 L’arrivée d’un train de potentiels d’action au niveau de la synapse neuromusculaire entraîne une ouverture des canaux calciques. Les ions Ca+ entrent dans la terminaison de l’axone et provoquent la libération de l’acétylcholine stockée dans les vésicules présynaptiques.
L’arrivée d’un train de potentiels d’action au niveau de la synapse neuromusculaire entraîne une ouverture des canaux calciques. Les ions Ca+ entrent dans la terminaison de l’axone et provoquent la libération de l’acétylcholine stockée dans les vésicules présynaptiques.
L’acétylcholine est libérée dans la fente synaptique et se fixe sur les récepteurs nicotiniques de la membrane post-synaptique (fibre musculaire). Ceci provoque l’ouverture des canaux sodiques qui provoque l’entrée de Na+ dans la fibre musculaire. Cela crée une dépolarisation à l’origine de la contraction musculaire.
Les molécules d’acétylcholine sont dégradées par l’acétylcholinestérase qui régule la contraction musculaire.
- La toxine botulique s’attaque au complexe SNARE qui permet la fusion des membranes vésiculaires et de la membrane axonale, permettant ainsi la libération de l’acétylcholine.
- Les curares et les anticorps de la myasthénie entrent en compétition avec l’acétylcholine au niveau des récepteurs nicotiniques, bloquant ainsi son action.
- Les anticholinestérasiques augmentent la concentration d’acétylcholine dans la fente synaptique.
Le codage en fréquence : les potentiels d’action du neurone moteur ont une amplitude constante. L’intensité de la contraction de la fibre musculaire dépend de la fréquence des potentiels d’action qui détermine la quantité d’acétylcholine libérée.
La contraction musculaire
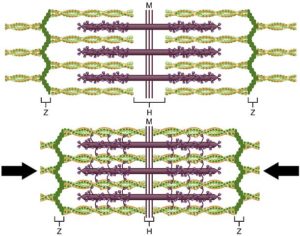 La dépolarisation de la fibre musculaire conduit à la libération de Ca+ par le réticulum sarcoplasmique. Le Ca+ se fixe sur l’actine, ce qui permet alors l’accrochage des têtes de myosine en regard. L’ATP se dégrade en ADP+P, ce produit l’énergie pour la flexion des ponts de myosine et le glissement des filaments : les sarcomères se raccourcissent. Les ponts de myosine sont enfin rechargés en ATP : ils se détendent et sont alors prêts pour un nouveau cycle.
La dépolarisation de la fibre musculaire conduit à la libération de Ca+ par le réticulum sarcoplasmique. Le Ca+ se fixe sur l’actine, ce qui permet alors l’accrochage des têtes de myosine en regard. L’ATP se dégrade en ADP+P, ce produit l’énergie pour la flexion des ponts de myosine et le glissement des filaments : les sarcomères se raccourcissent. Les ponts de myosine sont enfin rechargés en ATP : ils se détendent et sont alors prêts pour un nouveau cycle.
Le défaut de rechargement en ATP est responsable :
- Des contractures silencieuses dans la maladie de Mac Ardle : dysfonction de la phosphorylase nécessaire à la glycogénolyse musculaire
- De la rigidité cadavérique : fuite du calcium sarcoplasmique, arrêt des pompes ATPasique
Les neurones sensitifs
 La transmission sensitive depuis les récepteurs périphériques se fait par les neurones en T :
La transmission sensitive depuis les récepteurs périphériques se fait par les neurones en T :
- Les fibres périphériques sont les dendrites des neurones. Elles partent des récepteurs sensitifs cutanés, articulaires, musculaires ou des organes sensoriels
- Les corps cellulaires sont dans les ganglions sensitifs des racines nerveuses
- Les axones se poursuivent dans les racines et les voies médullaires
Les fibres sensitives périphériques sont classées en quatre groupes de fibres, dont trois sont myélinisées
- Groupe 1 : fibres myélinisées de gros calibre, pour la proprioception inconsciente
- Groupe 2 : moins de calibre plus faible pour la sensibilité tactile épicritique et la proprioception consciente
- Groupe 3 : de calibre plus faible et plus lentes pour la sensibilité thermiques
- Groupe 4 : fibres amyéliniques pour la douleur (fibres C)
En stimulodétection sensitive :
- On stimule et on recueille directement sur les fibres sensitives. Il n’y a pas de synapse périphérique, ce qui permet une mesure directe de la vitesse de conduction sensitive (VCS)
- On ne peut pas séparer les types de fibre. La réponse recueillie rend compte de l’ensemble des fibres. Elle est généralement assez étroite.
- Il n’y a pas d’exploration spécifique des fibres douloureuses.
Les ganglions sensitifs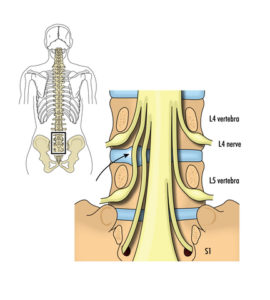
Ils forment un renflement de la racine dorsale des nerfs rachidiens
- A la partie latérale du foramen
- En situation normale, ils sont placés au-dessus de l’étage discal
Ils peuvent être comprimés par une hernie discale ascendante ou associée à un affaissement discal qui abaisse le pédicule sus-jacent (toit du foramen)
La vitalité des corps cellulaires conditionne la survie des fibres nerveuses sensitives
Dans une compression radiculaire avec anesthésie :
- Une persistance des réponses périphériques est en faveur d’une compression sus-ganglionnaire
- Une disparition des réponses périphériques laisse craindre une compression ganglionnaire et une persistance définitive des troubles sensitifs
Les voies sensitives en résumé
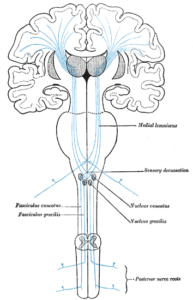
Gray’s anatomy – domaine public
La voie lemniscale (Goll et Burdach)
Elle véhicule la sensibilité consciente, tactile épicritique et proprioceptive.
Les axones du protoneurones sensitifs cheminent dans les racines puis dans les cordons postérieurs ipsi-latéraux de la moelle :
- Faisceau médial pour le membre inférieur
- Faisceau latéral pour le membre supérieur
La compression unilatérale de la moelle donne une hypoesthésie ipsilatérale à la lésion (comme pour une lésion radiculaire ou tronculaire).
Les synapses se font dans le bulbe, dans les noyaux de Goll et Burdach.
Les deutoneurones décussent juste au-dessus. Leur lésion donne alors des troubles sensitifs controlatéraux
Le deutoneurone fait relais dans le thalamus avec un 3ème neurone thalamocortical.
La voie spino-thalamique
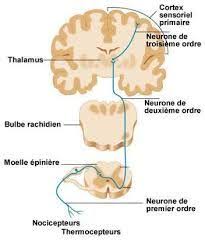 Le protoneurone fait relais dans la corne dorsale de la substance grise de la moelle
Le protoneurone fait relais dans la corne dorsale de la substance grise de la moelle
Le deutoneurone croise la ligne médiane en avant du canal épendymaire, au même étage métamérique. Il constitue le faisceau spino-thalamique opposé de la moelle et du tronc cérébral.
Il se termine dans les noyaux diffus non spécifiques du thalamus. On distingue deux contingents médullaires :
- Néo-spino-thalamique : sensibilité thermique et douleur, véhiculés par un 3ème neurone thalamo-cortical
- Paléospinothalamique pour le tact protopathique, distribué par un réseau multisynaptique
En exploration électrophysiologique
Les réponses sensitives disparaissent :
- Si lésion axonale tronculaire
- Si lésion du ganglion rachidien
Les réponses sensitives périphériques persistent :
- Au-dessous d’un bloc de conduction myélinique
- Si lésion radiculaire au-dessus d’un ganglion rachidien
Les fibres sensitives sont plus sensibles à la compression que les fibres motrices. Elles seront donc les premières atteintes :
- Dans les syndromes canalaires et les traumas mineurs
- Dans les compressions radiculaires
Les potentiels évoqués somesthésiques :
- Explorent bien les cordons postérieurs médullaires. Ils sont très utiles pour explorer la SEP et les myélopathies cervicarthrosiques
- Explorent mal les racines nerveuses